醫療器材服務
Medical Device Service
服務窗口
醫療器材 驗證 / 測試 / 安全性評估 / 生物相容性 / 生物相容性試驗
生物相容性試驗 [總論] (ISO 10993-1: 2018)
生物相容性 (ISO 10993)
執行生物相容性試驗主要為確保直接或間接接觸人體的產品 (如醫療器材、原料、化粧品…),不會於使用期間釋放有毒物質,造成局部或全身性的細胞毒性、致癌性或生殖毒性; 導致人體在接觸後引起發炎、免疫、毒性反應、溶血、血栓形成反應等危害。
 ISO 10993 涵蓋內容
ISO 10993 涵蓋內容
您知道2018年10月ISO 已正式公告ISO 10993-1的更新版內容了嗎?
ISO 10993-1:2018
Biological evaluation of medical devices -- Part 1: Evaluation and testing within a risk management process
◎ 2018年10月發行的ISO 10993-1最新版本對於生物性評估原則有確切的規範,其主要變更如下,塑膠中心已將新版要求納入委託試驗物質的生物性評估規劃中,歡迎有興趣深入了解的廠商與我們進一步聯繫。
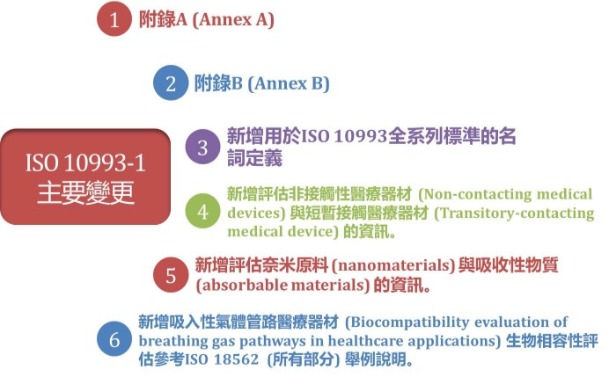 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點
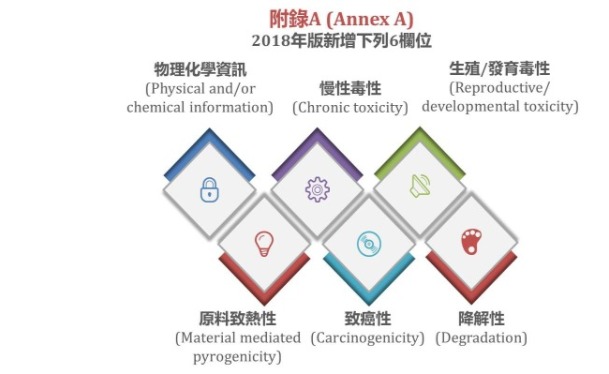 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點
 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點
 生物相容性測試(Biocompatibility Test)- ISO 10993-1:2018/USP/OECD
生物相容性測試(Biocompatibility Test)- ISO 10993-1:2018/USP/OECD
 ISO 10993 涵蓋內容
ISO 10993 涵蓋內容 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點 ISO 10993-1:2018改版重點
ISO 10993-1:2018改版重點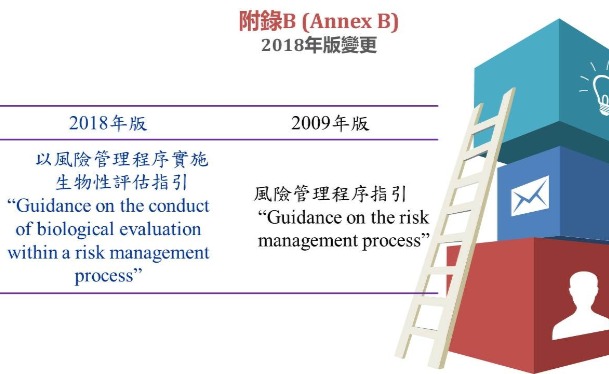
 生物相容性測試(Biocompatibility Test)- ISO 10993-1:2018/USP/OECD
生物相容性測試(Biocompatibility Test)- ISO 10993-1:2018/USP/OECD
